ОПРЕДЕЛЕНИЯ ОКИСЛЕНИЯ (OXIDATION) И РЕДУКЦИЯ (REDUCTION) (РЕДОКС)
Оригинальная статья: DEFINITIONS OF OXIDATION AND REDUCTION (REDOX)
Автор статьи: Джим Кларк (Jim Clark)
Источник: https://www.chemguide.co.uk/inorganic/redox/definitions.html
На этой странице рассматриваются различные определения окисления и редукция (окислительно-восстановительные) в терминах переноса кислорода, водорода и электронов. Он также объясняет термины окисляющий агент и восстанавливающий агент.
Окисление и редукция с точки зрения переноса кислорода
Определения
-
Окисление - это увеличение кислорода.
-
Редукция - это потеря кислорода.
Например, при добыче железа из его руды:
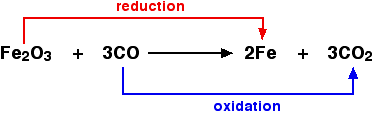
Поскольку и восстановление, и окисление идут бок о бок, это известно как окислительно-восстановительная реакция.
Окисляющие и восстановители
Окислителем является вещество, которое окисляет что-то еще. В приведенном выше примере оксид железа (III) является окислителем.
Редуктор уменьшает что-то еще. В уравнении монооксид углерода является восстановителем.
-
Окисляющие агенты дают кислород другому веществу.
-
Редукторы удаляют кислород из другого вещества.
Окисление и редукция в условиях переноса водорода
Это старые определения, которые в наши дни не используются.Наиболее вероятное место, где вы встретитесь, - это органическая химия.
Определения
-
Окисление - это потеря водорода.
-
Редукция - это увеличение содержания водорода.
Обратите внимание, что это точно противоположно определениям кислорода.
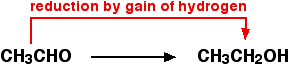
Например, этанол может быть окислен до этанала:

Вам нужно будет использовать окислитель для удаления водорода из этанола. Обычно используемым окислителем является раствор дихромата калия (VI), подкисленный разбавленной серной кислотой.
Этанал также можно снова вернуть к этанолу, добавив к нему водород. Возможным восстановителем является тетрагидриборат натрия, NaBH4. Опять же, это слишком сложное уравнение, которое стоит потрудиться на этом этапе.
Обновление окислителей и восстановителей
-
Окислители подают кислород другому веществу или удаляют из него водород.
-
Редукторы удаляют кислород из другого вещества или дают ему водород.
Окисление и редукция с точки зрения переноса электрона
Это очень простое использование терминов окисления и восстановления на уровне А '.
Определения
-
Окисление - это потеря электронов.
-
Редукция - это усиление электронов.
Очень важно помнить эти определения. Это очень простой способ сделать это. Пока вы помните, что речь идет о переносе электрона:
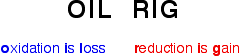
Простой пример
Уравнение показывает простую окислительно-восстановительную реакцию, которая, очевидно, может быть описана в терминах переноса кислорода.
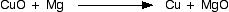
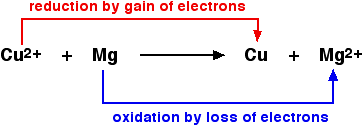
Оксид меди (II) и оксид магния являются ионными. Очевидно, что металлов нет. Если вы перепишете это как ионное уравнение, то окажется, что ионы оксида являются ионами зрителей, и вы остаетесь:
Последний комментарий к окислителям и восстановителям
Если вы посмотрите на приведенное выше уравнение, магний уменьшает ионы меди (II), давая им электроны для нейтрализации заряда. Магний является восстановителем.
Взглянув на него наоборот, ионы меди (II) удаляют электроны из магния для создания ионов магния. Ионы меди (II) действуют как окислитель.
Предупреждение!
Это потенциально очень запутанно, если вы попытаетесь узнать, как окисление и сокращение означают с точки зрения переноса электрона, а также изучать определения окислителей и восстановителей в тех же условиях.
Лично я бы порекомендовал вам работать, если вам это нужно.Аргумент (происходящий внутри вашей головы) пойдет так, если вы хотите узнать, например, что окислитель сделал с точки зрения электронов:
-
Окислитель окисляет что-то еще.
-
Окисление - это потеря электронов (OIL RIG).
-
Это означает, что окислитель извлекает электроны из этого другого вещества.
-
Поэтому окислитель должен получить электроны.
Или вы могли бы подумать так:
-
Окислитель окисляет что-то еще.
-
Это означает, что окислитель должен быть уменьшен.
-
Уменьшение - усиление электронов (OIL RIG).
-
Поэтому окислитель должен получить электроны.
Понимание гораздо безопаснее, чем бездумное обучение!